Marihuana tradicional, cannabis de alta potencia y cannabinoides sintéticos: aumento del riesgo de psicosis
Robin M. Murray, 1 Harriet Quigley, 1 Diego Quattrone, 1 Amir Englund, 1 y Marta Di Forti 1
1Instituto de Psiquiatría, Psicología y Neurociencia, King's College, Parque De Crespigny, Londres, SE5 8AF, Reino Unido
ABSTRACT
La evidencia epidemiológica demuestra que el consumo de cannabis está asociado con un mayor riesgo de brotes psicóticos y confirma una relación dosis-respuesta entre el uso y el riesgo de psicosis. El cannabis de alta potencia y los cannabinoides sintéticos generan el mayor riesgo. La administración experimental de tetrahidrocannabinol, el ingrediente activo del cannabis, induce psicosis transitoria en sujetos normales, pero este efecto se puede reducir mediante la administración concomitante de cannabidiol. Este último es un componente del hachís tradicional, pero está en gran parte ausente en las formas modernas de cannabis de alta potencia. El argumento continúa sobre la medida en que la predisposición genética se correlaciona con el consumo de cannabis, o interactúa con él, y qué proporción de la psicosis podría prevenirse minimizando el uso intensivo del cannabis. Hasta el momento, no hay pruebas convincentes de que el consumo de cannabis aumenta el riesgo de otros trastornos psiquiátricos, pero no existen dudas sobre su efecto perjudicial sobre la función cognitiva. Todos los aspectos negativos se magnifican si el uso comienza en la adolescencia temprana. Independientemente de si el consumo de cannabis sea descriminalizado o legalizado, la evidencia de que es una causa componente de psicosis es ahora suficiente para la emisión de mensajes de salud pública que describan el riesgo, especialmente del consumo constante de cannabis de alta potencia y cannabinoides sintéticos.
Palabras clave: Cannabis, psicosis, marihuana, cannabinoides sintéticos, función cognitiva, estructura cerebral, predisposición genética, adolescencia temprana
El uso del cannabis ha sido ilegal en la mayoría de los países desde la década de 1930, pero esto no ha disuadido el uso1. En la actualidad, el cannabis es utilizado por alrededor de 180 millones de personas en todo el mundo2. Las tensiones producidas por esta situación insatisfactoria han dado lugar a que se preste mucha atención al estatuto jurídico del cannabis.
La posesión de la droga en pequeñas cantidades se ha despenalizado oficialmente en países como Portugal y los Países Bajos, y extraoficialmente en muchos más. En 2013, Uruguay se convirtió en la primera nación en legalizar la venta, cultivo y distribución de cannabis3. Cuatro estados de Estados Unidos también han legalizado el uso recreativo, y otros veinticinco estados de los Estados Unidos, así como Canadá, permiten la "marihuana medicinal". Mientras que Uruguay tiene reglas estrictas referentes al acceso, las leyes varían de estado a estado en los Estados Unidos, con la política impulsada cada vez más por los empresarios en busca de beneficios, y los legisladores en busca de impuestos.
CANNABINOIDES Y EL SISTEMA ENDOCANNABINOIDE
El cannabis contiene más de un centenar de cannabinoides4, siendo los más importantes el tetrahidrocannabinol (THC) y el cannabidiol (CBD). Éstos se producen en formaciones cristalinas minúsculas en las partes altas de las flores. El cannabis recreativo ha sido tradicionalmente disponible como hierba (marihuana, hierba, mota) o resina (hashish, hash). En algunos países como los Estados Unidos se fuman solos, mientras que en gran parte de Europa se fuma con tabaco. Cuando se fuman o se inhalan, los efectos se activan después de unos minutos y duran de 2 a 3 horas; Si se come, puede tardar 2 horas para que los efectos se sientan y pueden durar hasta 8 horas.
Los cannabinoides ejercen sus efectos principalmente al interactuar con el sistema endocannabinoide, que comprende ligandos endógenos, sus receptores y las enzimas que los sintetizan y degradan5.
Existen dos receptores específicos: el receptor cannabinoide tipo 1 (CB1) y el receptor cannabinoide tipo 2 (CB2). El receptor CB1 está muy extendido en todo el cerebro, con altas concentraciones en el neocórtex, los ganglios basales y el hipocampo6. Los receptores CB1 se localizan pre-sinápticamente en los terminales de las neuronas GABAérgicas y glutamatérgicas, donde actúan homeostáticamente para contrarrestar la sobre o subactividad de estos sistemas, modulando la liberación de neurotransmisores pre-sinápticos7. El receptor CB2, inicialmente pensado como confinado a células inmunes y tejidos periféricos8, también se ha encontrado recientemente en el cerebelo y el tronco encefálico.
Los ligandos de los receptores cannabinoides endógenos más conocidos son N-araquidonoiletanolamida (anandamida, AEA) y 2-araquidonoilglicerol (2-AG). Éstos son biosintetizados post-sinápticamente de manera dependiendo de la actividad antes de ser despejados por un mecanismo de recaptación e hidrólisis enzimática.
El THC es responsable de la euforia y los sentimientos de mayor sociabilidad y perspicacia, "el subidón" que disfrutan los usuarios. Es un agonista parcial en el receptor CB1. Dado que el sistema endocannabinoide normalmente opera "bajo demanda" de una manera dependiente de la actividad10, el THC exógeno parece abrumar el sistema endógeno 11, 12, 13, 14, 15, con los niveles resultantes inferiores, por ejemplo, de AEA1
La administración de THC a voluntarios sanos afecta el aprendizaje, la atención y la memoria de una manera dosis-respuesta17, 18, 19, 20, 21, 22. Tal deterioro es probablemente por qué los conductores, bajo la influencia del cannabis, corren el doble de riesgo de sufrir accidentes de tránsito23. Los estudios experimentales también han demostrado que una dosis suficientemente alta de THC intravenoso puede inducir síntomas psicóticos de corta duración, incluyendo paranoia y alucinaciones19, 24, 25. También aumenta los pensamientos paranoicos en un entorno de realidad virtual26.
El CBD carece de afinidad significativa para el receptor CB1 27, 28, pero es capaz de desplazar el THC a bajas concentraciones a nivel nanomolar29. Puede actuar de forma antagonista contra agonistas CB1 a través de un sitio de unión no ortoestérico30. Parece bloquear o mejorar muchos de los efectos del THC. Por ejemplo, la coadministración de CBD reduce significativamente la taquicardia inducida por THC31, los efectos ansiogénicos de THC32 y los efectos perjudiciales del THC sobre la percepción33, 34 y la memoria35.
La naturaleza cambiante de los Cannabinoides recreativos
La proporción de THC en las flores de cannabis(marihuana) y resina (hachís) de uso común era de 3% o menos en los años sesenta, pero comenzó a aumentar posteriormente. Los cultivadores cruzaron las plantas para aumentar la potencia. Luego, encontraron que la prevención de la polinización aumentaba el THC, ya que en esta situación la planta femenina convierte su energía en producir más cannabinoides en lugar de semillas36. Este tipo de cannabis se conoce como sinsemilla, que significa "sin semilla" en español, pero a veces se conoce coloquialmente como "skunk", debido a su fuerte olor. Las plantas criadas para producir una alta concentración de THC no pueden producir simultáneamente gran cantidad de CBD, por lo que el producto contiene sólo trazas de este último37.
En los primeros años del siglo XXI, la proporción media de THC había aumentado a 16 y 20% en Inglaterra y Holanda respectivamente, y la sinsemilla había tomado gran parte del mercado tradicional de la resina37,38. Con una media de THC en torno al 15% 39, mientras que en los EE.UU. la potencia alcanzó un promedio de 12% en 201440.
En los Estados Unidos, donde se ha legalizado el cannabis recreativo o la "marihuana medicinal", una variedad cada vez más amplia de productos están disponibles, incluyendo aceites y comestibles, como galletas, chocolates y pasteles. Nuevas formas de extraer THC de la planta han producido aceite de resina con un contenido de THC de hasta el 80%, mientras que otras innovaciones que ofrecen altas concentraciones de THC incluyen vaping y dabbing.
J.W. Huffman pasó más de 25 años buscando sintetizar cannabinoides para uso terapéutico41. Sin embargo, a finales de los años 2000, algunos de sus compuestos comenzaron a ser utilizados como "drogas legales", a menudo denominado "Spice". Mas tarde, el uso de estos cannabinoides sintéticos aumentó dramáticamente, a menudo rociándolo en mezclas de hierbas. Mientras que el THC es un agonista parcial con una afinidad débil para el receptor CB1, los cannabinoides sintéticos son agonistas completos y generalmente tienen mayor afinidad. No es sorprendente que supongan un mayor riesgo para la salud comparado con el cannabis de las plantas42,43,44. Una encuesta de 80,000 consumidores mostró que los que consumían cannabinoides sintéticos tenían treinta veces más probabilidades de terminar en una unidad de emergencia que los usuarios de cannabis tradicional45. Las reacciones físicas agudas incluyen náuseas y vómitos, disnea, hipertensión, taquicardia, dolor torácico y ocasionalmente insuficiencia renal aguda.
Se han reportado más de 200 cannabinoides sintéticos en Internet46. Como cada uno tiene una estructura molecular ligeramente diferente, pueden tener efectos secundarios impredecibles. Además, no pueden ser detectados por las pruebas de drogas de rutina, haciéndolas particularmente atractivas para las personas encarceladas y en el ejército.
Psicosis
La preocupación de que el consumo de cannabis pueda inducir psicosis no es nueva. Por ejemplo, en 1896, el psiquiatra escocés T. Clouston visitó un asilo en El Cairo y señaló que 40 de 253 personas en el hospital presentaban locura atribuida al uso del hashish47. Sin embargo, en la década de 1960, este punto de vista era comúnmente ridiculizado como "locura de puestés", con la implicación de que eran los que creían que el cannabis podría inducir a la psicosis a las personas que estaban locos, en lugar de los que consumieron la droga.
En el primer estudio prospectivo para explorar si el cannabis jugó un papel causal en la psicosis, Andréasson et. al.48 rastrearon a 45,750 jóvenes a los que se les había preguntado sobre su consumo de drogas cuando fueron reclutados en el ejército sueco. Aquellos que habían consumido cannabis más de cincuenta veces tenían seis veces más probabilidades de desarrollar esquizofrenia en los próximos quince años que aquellos que nunca lo habían usado. Sorprendentemente, los resultados fueron ignorados en su mayoría. Incluso The Lancet, que publicó el trabajo de Andréasson et al en 1987, publicó un editorial en 1995 en el que se afirmaba la opinión predominante de que "fumar cannabis, incluso a largo plazo, no es perjudicial para la salud" 49.
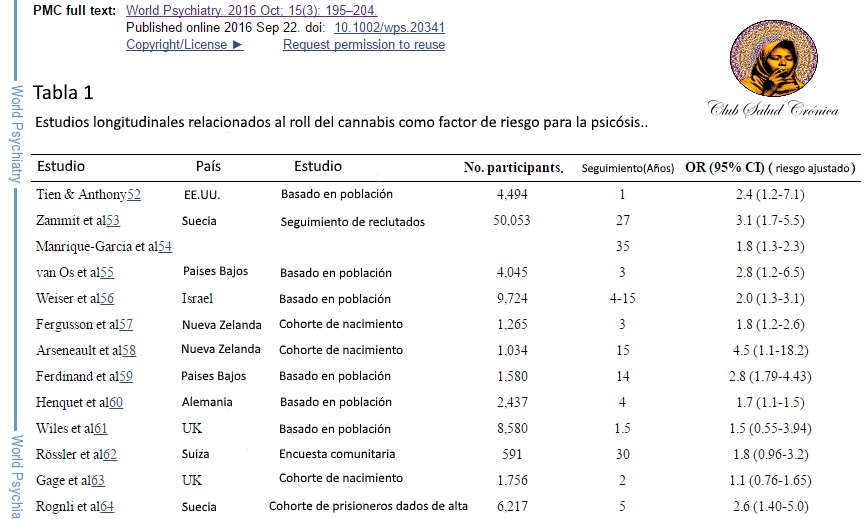
Sin embargo, ha habido una serie de estudios prospectivos longitudinales50, 51. Nueve de cada doce encontraron que el consumo de cannabis se asoció con un riesgo significativamente mayor de síntomas psicóticos o de enfermedad psicótica; los tres restantes mostraron una tendencia en la misma dirección52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64 (Tabla 1). Marconi et al65 realizaron un meta-análisis y demostraron que cuanto mayor es el consumo de cannabis, mayor es el riesgo de psicosis en todos los estudios incluidos. Hubo un ratio OR de casi cuatro para el riesgo de los resultados relacionados con la psicosis entre los usuarios más fuertes en comparación con los no usuarios.
¿Es más arriesgado el uso de tipos de cannabis con mayor potencia que las tradicionales? Di Forti et al66 examinaron 410 pacientes con su primer episodio de trastorno psicótico y 390 controles sanos. Las personas que consumían cannabis con alta potencia diariamente tenían cinco veces más probabilidades de padecer un trastorno psicótico que los no usuarios. El uso de hachís no estuvo relacionado con un mayor riesgo de psicosis, posiblemente debido a su menor contenido de THC combinado con la presencia de CBD66, 67, 68.
Del mismo modo, en una encuesta holandesa de 2.000 usuarios de cannabis, los que preferían el cannabis con el contenido más alto de CDB habían experimentado menos experiencias psicóticas69. Morgan y Curran70, quienes testearon el cabello para los cannabinoides, mostraron que los usuarios con THC y CBD detectables tenían menos síntomas psicóticos que aquellos con sólo THC. Finalmente, en un estudio experimental de 48 voluntarios sanos, el tratamiento con CBD oral antes de la administración de THC intravenoso redujo significativamente la aparición de síntomas psicóticos35.
Han comenzado a surgir casos de psicosis tras el uso de tipos de cannabis con un contenido de THC mucho más elevado, por ejemplo, "wax dabs" 71. Los síntomas psiquiátricos también son cada vez más reportados como consecuencia del uso de cannabinoides sintéticos72. Papanti et al73 realizaron una revisión sistemática e informaron que la agitación, la ansiedad, la paranoia y la psicosis pueden presentarse; estas reacciones a veces se conocen como "spiceofrenia". La creciente evidencia sugiere que pueden producirse trastornos psicóticos más crónicos en los usuarios persistentes de cannabinoides sintéticos74.
La existencia de una "psicosis del cannabis" distinta de la esquizofrenia es dudosa. Es cierto que un alto consumo repentino puede inducir un estado de intoxicación aguda que normalmente se resuelve rápidamente. Esto no es infrecuente con el consumo de comestibles, donde es más difícil valorar la dosis que con el cannabis fumado. El uso de cannabinoides vegetales o sintéticos durante un tiempo relativamente corto puede inducir una psicosis aguda de la que las personas se recuperan durante un período de días o semanas. Pero cuanto más tiempo se prolonga, más se fusiona el cuadro clínico con el de la esquizofrenia-psicosis54, 64.
Sin embargo, hay diferencias entre las personas con una psicosis asociada al cannabis y los pacientes psicóticos que no la consumieron. Los pacientes que consumen cannabis tienden a tener un inicio significativamente más temprano que los pacientes con psicosis que nunca consumieron cannabis75. Un estudio mostró una asociación dosis-respuesta con usuarios diarios de cannabis de alta potencia experimentando su primer episodio de psicosis, en promedio, 6 años más jóvenes que los nunca usuarios68.
Los pacientes psicóticos que consumen cannabis también tienden a tener un coeficiente de inteligencia superior y una mejor neuro-cognición que los pacientes psicóticos que no usan76, 77. Tienen también un mayor IQ premórbido y una mejor función social premórbida78 y tienen menos probabilidades de mostrar signos neurológicos suaves79. La explicación probable es que muchos pacientes esquizofrénicos que no usan drogas tienen algún deterioro del neurodesarrollo y consecuentemente mala cognición premórbida y función social. En cambio, los que han consumido cannabis a menudo son inteligentes y sociables; introducidos al cannabis por sus amigos, son lo suficientemente sociables para poder ocultar su hábito a sus padres.
Críticos de la hipótesis sobre el causal
La mayoría de los expertos europeos y australianos están convencidos de que el cannabis es una de las causas que contribuyen a la esquizofrenia. Sin embargo, tres artículos escépticos han aparecido recientemente de EE.UU.80, 81, 82. Ahora revisaremos las principales críticas.
Una insinuación a ha sido que aquellos que consumen cannabis pueden ser psicológicamente más vulnerables que aquellos que no lo hacen. Sin embargo, el estudio de Dunedin de Nueva Zelanda controló síntomas psicóticos a la edad de 11 años, y de todos modos encontró un vínculo entre el uso de cannabis y síntomas psicóticos posteriores58.
¿Podría alguna gente tomar cannabis en un intento de automedicar los síntomas de la psicosis o sus precursores? Hay poca evidencia para esto. Un segundo estudio de Nueva Zelanda, esta vez de Christchurch, mostró que una vez que los síntomas psicóticos menores se desarrollaron, la gente tendía a fumar menos83. Además, cuando se pregunta a los pacientes psicóticos por qué usan cannabis, ellos reportan las mismas razones hedónicas que el resto de la población, es decir, para el disfrute84. De hecho, aunque muchos saben que desarrollarán ideas paranoicas, el "subidón" inmediato los supera.
Una sugerencia común ha sido que los usuarios de cannabis que son psicóticos también han consumido otras drogas. Sin embargo, varios estudios han abordado esta cuestión y no han encontrado el efecto suficiente para negar el impacto del cannabis58, incluso cuando se tomó en cuenta el uso de tabaco66,67.
Otro argumento indica que el consumo de cannabis se hizo más común en la última parte del siglo XX sin un cambio evidente en la incidencia de la esquizofrenia. De hecho, hay poca información confiable sobre las tendencias temporales en la incidencia de la esquizofrenia, por lo que es difícil saber si esto es cierto o no. El único estudio competente que abarcó varias décadas y que utilizó los mismos criterios de investigación para la esquizofrenia informó que la incidencia se duplicó entre 1965 y 1999 y que la proporción de pacientes esquizofrénicos que consumían cannabis aumentó de manera desproporcionada en comparación con otros pacientes psiquiátricos85.
¿Predisposición genética o interacción al medio ambiente del gen?
Una explicación popular acerca de la asociación entre el consumo de cannabis y la psicosis es la vulnerabilidad genética compartida80, 81, 86. Los pacientes psicóticos que consumen cannabis no suelen tener otros parientes que sean psicóticos87. Sin embargo, a menudo otros miembros psicóticos de la familia también usan cannabis
Ahora se puede examinar la relación entre la predisposición a la psicosis, medida por la puntuación de riesgo poligénico para la esquizofrenia y el consumo de cannabis. Power et al.88 examinaron el efecto del resultado del riesgo poligénico en el uso de cannabis en una gran muestra de australianos. La puntuación fue responsable de sólo una proporción muy pequeña del consumo de cannabis. De manera similar, Gage et al89 sugirieron que aquellos que utilizaban cannabis de alta potencia podrían estar especialmente predispuestos genéticamente a la psicosis. Sin embargo, Di Forti et al90, que examinó el nivel de riesgo poligénico en la esquizofrenia en los usuarios de cannabis de baja y alta potencia, no encontraron evidencia que respalde este punto de vista.
Una posibilidad más probable es que algunos individuos son más vulnerables a los efectos psicotogénicos del cannabis que otros. Ningún estudio publicado ha examinado todavía una posible interacción entre el nivel de riesgo poligénico para la esquizofrenia y el consumo de cannabis en la causa de la psicosis. Sin embargo, los pacientes de esquizofrenia con grandes y raras deleciones son menos propensos a tener abuso de cannabis comórbido durante su vida que aquellos sin tales variantes91. Esto proporciona apoyo para un modelo de riesgo umbral, con aquellos que llevan una copy number variant que necesitan menos exposiciones ambientales adversas para convertirse en, francamente, psicóticos.
Otros trabajos han examinado genes candidatos involucrados en el sistema de dopamina. Caspi et al92 sugirió que variaciones en el gen de la catecol-O-metiltransferasa (COMT) podría moderar labilidad a la psicosis inducida por cannabis, pero los intentos para reproduciros han sido inconsistentes. Más recientemente, un estudio experimental93 no encontró ningún efecto de este polimorfismo COMT en síntomas psicóticos inducidos por THC, pero aquellos con el genotipo val / val tuvieron un mayor decremento en la memoria mecánica(working memory).
Dos estudios de control de caso han informado de que una variante de AKT1 aumenta el riesgo de enfermedad psicótica entre los consumidores de cannabis y un tercero ha demostrado que los que portan esta variante muestran una mayor respuesta psicotogénica al cannabis fumado94, 95, 96. Otro informe indica que un variante en el gen receptor D2 también puede aumentar el riesgo de psicosis, y que el riesgo es aún mayor en los portadores de esta variante y el polimorfismo AKT1 mencionado anteriormente97.
¿Cuál es el mecanismo de acción?
Bianconi et al84 mostraron que los pacientes psicóticos que consumían cannabis parecían ser más sensibles tanto a los efectos positivos como negativos del fármaco. Hallazgos similares han sido reportados en individuos con alto riesgo clínico de desarrollar psicosis98. D'Souza et al24 mostraron que las personas con esquizofrenia tenían una reacción más fuerte a los efectos psicotogénicos y cognitivos del THC intravenoso en comparación con controles sanos.
En estudios con animales, la administración de THC confiablemente conduce a una mayor liberación de dopamina, pero los estudios en seres humanos han sido más equívocos. Un estudio de tomografía de emisión de positrones (PET) informó un aumento en la liberación de dopamina estriatal, pero otro no encontró efecto significativo. Un re-análisis que combina los datos de los dos estudios informó un pequeño pero significativo aumento en la liberación de dopamina inducida por el THC99.
Varios estudios de PET han demostrado que los usuarios de cannabis, al igual que otros consumidores de drogas, tienen una baja capacidad para sintetizar y liberar dopamina estriada. Sin embargo, Volkow et al100 informó que, a diferencia de otros toxicómanos, los usuarios de cannabis no muestran alteración en los receptores D2 / D3 estriados. Además, tras una prueba con anfetaminas, los pacientes psicóticos que consumen cannabis, a pesar de la ausencia de marcada elevación en la liberación de dopamina, presentan una mayor exacerbación de sus síntomas en comparación con los pacientes que nunca lo usaron. Estos hallazgos podrían ser explicados por el uso de cannabis que induce la supersensibilidad de la dopamina post-sináptica101, como lo encontraron Ginovart et al102 en su estudio de animales que recibieron THC permanentemente. Esta hipótesis se ve reforzada por la evidencia genética, revisada anteriormente, de que la variación en los genes post-sinápticos puede predisponer a la psicosis asociada al cannabis.
Resultados y Tratamiento
Un meta-análisis reciente mostró que los pacientes psicóticos que continuaron con el consumo de cannabis tuvieron tasas de recaída más altas, ingresos hospitalarios más largos y síntomas positivos más graves que los antiguos usuarios que interrumpieron el consumo o los que nunca consumieron103.
Desafortunadamente, persuadir a los usuarios de cannabis detenerse no es fácil. Se han intentado una variedad de terapias, especialmente la terapia cognitivo-conductual y la entrevista motivacional, pero hasta ahora no han tenido mucho éxito. Actualmente se están realizando ensayos con tokens para limpiar el cannabis en la orina. El único tratamiento farmacológico que ha tenido éxito es la clozapina: un ensayo doble-ciego demostró que tiene un efecto útil para disminuir el antojo de cannabis104.
Otros transtornos psiquiátricos

Crédito de la foto: Instagram
Dependencia del cannabis
Los síntomas de abstinencia suelen ser relativamente menores, ya que el cannabis permanece en el cuerpo durante varias semanas. Sin embargo, la ansiedad y el antojo, la irritabilidad, el insomnio, trastornos del apetito, disforia y depresión se pueden presentar.
Casi el 10% de los usuarios se convertirán en dependientes105, 106, y algunos afirman que la tasa va tan alto como un 17% si el uso comienza en la adolescencia107. Ciertamente, la dependencia al cannabis es una causa cada vez más frecuente de búsqueda de ayuda en Australia, Reino Unido, Europa continental y América del Norte23, 108. Una encuesta en Internet109 informó que el consumo de cannabis de alta potencia estaba asociado con un aumento de la probabilidad de dependencia.
Depresión y trastornos de ansiedad
Estudios transversales reportan una alta prevalencia de trastornos de depresión y ansiedad en los usuarios de cannabis110, 111, 112, 113, pero la dirección del efecto sigue siendo incierta112, 114, 115, 116.
El seguimiento de conscriptos suecos no mostró evidencia de un mayor riesgo de depresión en los usuarios de cannabis117, y las revisiones sistemáticas han proporcionado sólo evidencia débil de que el uso de cannabis aumenta el riesgo de resultados afectivos118, 119. Sin embargo, una revisión concluyó que el consumo de cannabis estaba asociado con un modesto aumento en el riesgo de depresión, y el uso constante explicaría un riesgo ligeramente más fuerte120.
Por otra parte, un estudio prospectivo de gran cohorte estadounidense encontró que el consumo de cannabis se asoció con mayores probabilidades de consumo de alcohol, nicotina y otras drogas, pero no de trastornos de ánimo o ansiedad121.
Trastorno de estrés postraumático
Las personas con trastorno de estrés postraumático (TEPT) son especialmente propensas a consumir cannabis122, 123, 124, pero nuevamente la naturaleza de esta relación es incierta. Algunos estudios muestran que las experiencias traumáticas y el posterior PTSD aumentan el riesgo de abuso de drogas125, 126.
El cannabis se ha vuelto popular entre los veteranos militares estadounidenses que sufren de trastorno de estrés postraumático, y varios estados de los Estados Unidos han aprobado su uso medicinal para tales síntomas. Sin embargo, hasta el momento no hay pruebas sobre la seguridad o la eficacia de esta práctica.
Desorden hiperactivo y deficit de atencion
Existe una alta prevalencia de trastorno por déficit de atención / hiperactividad (ADHD) en adultos que buscan tratamiento para el uso de cannabis127. Estudios prospectivos muestran que el consumo de cannabis aumenta el riesgo de ADHD128 adulto, mientras que la hiperactividad / impulsividad infantil predice el consumo precoz de sustancias129.
Sigue siendo controvertido si el uso medicinal de cannabis reduce el uso de medicación estimulante. Un pequeño ensayo controlado con placebo en adultos con TDAH está en curso130.
Resumen
La evidencia de que el consumo de cannabis aumenta el riesgo de depresión, trastornos de ansiedad, trastorno de estrés postraumático o TDAH es mucho menos convincente que la de la psicosis. De hecho, sigue siendo posible, pero no probado, que el cannabis puede ser útil para las personas con TEPT y TDAH.
Efectos en el cerebro y en la cognición.
Hay muchos informes sobre que el consumo de cannabis puede alterar la estructura cerebral. Sin embargo, muchos de los estudios son pequeños, los grupos de control son inadecuados y la mayoría no han controlado completamente los efectos del consumo de alcohol (los usuarios de cannabis pesados también tienden a ser usuarios frecuentes de alcohol)131.
Dos grandes estudios recientes no encontraron ningún efecto principal del cannabis sobre la estructura cerebral132, 133. Sin embargo, el estudio anterior132 destaca que los investigadores encontraron una interacción con el indice de riesgo poligénico para la esquizofrenia, de tal forma que los individuos con un nivel de poligeno alto (pero no bajo) que utilizó cannabis mostró un grosor cortical disminuido. Por lo tanto, las personas con una vulnerabilidad a la esquizofrenia también pueden ser más vulnerables a los efectos adversos del cannabis en el cerebro.
Generalmente, la potencia no se ha tenido en cuenta en los estudios de imagenología. Sin embargo, Yucel et al134 encontró que aquellos que usaban cannabis de alta potencia mostraron decrementos de volumen del hipocampo, mientras que aquellos que habían usado preparaciones que contenían CBD no lo hicieron. Del mismo modo, en otro estudio con muestras de pelo, los usuarios de cannabis con registro más alto en CBD muestran menos decremento en el volumen del hipocampo derecho que los usuarios con menos CBD135. Otro estudio de resonancia magnética encontró que el uso de cannabis de alta potencia estaba asociado con conexiones distorsionadas en la sustancia blanca en el cuerpo calloso, un efecto que estaba ausente en los usuarios de hashish136.
Los usuarios de cannabis tienen peores resultados en función ejecutiva, atención, habilidad verbal y tareas de memoria que los no usuarios137, 138. El seguimiento de Dunedin mostró una disminución en las puntuaciones de IC de seis puntos entre las edades de 13-38 entre los que habían sido diagnosticados repetidamente con trastornos por uso de cannabis139. Recientemente, en un estudio de seguimiento con 5.115 hombres y mujeres jóvenes durante 25 años, la exposición pasada a la marihuana se asoció con una memoria verbal peor, pero no parecía afectar la función ejecutiva o la velocidad del procesamiento142.
Como recientemente ha sido resumido por Hall y Lynskey143, "estudios de controles de caso generalmente han encontrado un menor aprendizaje verbal, memoria y atención en aquellos que usan marihuana con regularidad con controles; el tamaño de estas diferencias por lo general se ha relacionado con la duración y la frecuencia de uso de cannabis". Algunos estudios sugieren que la cognición puede recuperarse completamente cuando el uso se detiene144, mientras que otros indican que sólo es posible la recuperación parcial142.
Una vez más, el CBD puede mejorar el impacto negativo del THC. Un estudio naturalista con 134 usuarios encontró que los participantes que consumían cannabis más alto en CBD no mostraban deterioro cognitivo145. El mismo grupo exploró el funcionamiento de la memoria en 120 usuarios: los participantes cuyo cabello daba positivo para CBD y THC mostraron un rendimiento significativamente mejor que aquellos con sólo THC146.
¿Son los adolescentes especialmente vulnerables?
Algunos estudios de imagen cerebral han encontrado mayores cambios cerebrales en aquellos que comenzaron el uso intensivo de cannabis en la adolescencia en comparación con la vida adulta, incluyendo disminución de volumen en varias regiones corticales y subcorticales, junto con evidencia de alteración de la sustancia blanca y respuestas anormales de activación cerebral a tareas cognitivas138. Estos informes esperan confirmación.
Pope et al147 encontró que el inicio del consumo de cannabis antes de los 17 años se asoció con menores puntuaciones verbales de CI en los usuarios de cannabis alto en THC a largo plazo. También hubo una mayor disminución del coeficiente de inteligencia en aquellos miembros de la cohorte de Dunedin que comenzaron a usarlos en la adolescencia148, pero el declive social no fue tan asociado con la edad de inicio149.
Silins et al150 revisaron a 2.500 jóvenes en Australasia y encontraron que el consumo diario de cannabis antes de los 17 años se asociaba con "claras reducciones" en la probabilidad de terminar la escuela secundaria y obtener un título universitario. Del mismo modo, un seguimiento de 1 año de 1.155 adolescentes encontró que el consumo semanal de cannabis se relaciona con el menor rendimiento en matemáticas y pruebas de Inglés151.
En el informe original de la cohorte de Dunedin sobre la psicosis, los que empezaron a consumir cannabis a los 18 años o más tarde mostraron sólo un pequeño aumento no significativo del riesgo de psicosis esquizofrénica a los 26 años, pero el riesgo aumentó cuatro veces entre los reclutados a partir de los 15 años o menos58.
Una posible explicación de los informes anteriores es que el cerebro todavía está en desarrollo en aquellos que comienzan el cannabis en la adolescencia. Exponer el cerebro juvenil a la droga podría perjudicar permanentemente el sistema endocannabinoide, e impactar negativamente sobre el cerebro y la función del neurotransmisor138.
Uso terapéutico del cannabis y sus componentes.
Los problemas relacionados con el uso recreativo del cannabis no deben cegarnos a la posibilidad de que algunos de sus componentes puedan tener efectos terapéuticos útiles, como por ejemplo, con los opiáceos.
Un ensayo clínico alemán152 encontró que el CBD tenía acciones antipsicóticas equivalentes a un antipsicótico estándar, amisulprida, en pacientes con esquizofrenia. Además, en un estudio de pacientes psicóticos que sólo respondían parcialmente a los antipsicóticos, la adición de CBD en lugar de placebo llevó a una mejora significativa en la puntuación en una escala de psicosis153.
Los receptores de cannabinoides modulan la percepción del dolor, por lo que no es sorprendente que haya informes de uso terapéutico de cannabinoides exógenos en el dolor humano. Se ha informado del efecto beneficioso del THC inhalado en el dolor de la neuropatía asociada al VIH154, y se encontró que proporciona alivio a corto plazo del dolor neuropático crónico, con un número necesario de tratar de 5.6155.
Ya se dispone de varios fármacos cannabinoides. Por ejemplo, el THC se ha utilizado durante mucho tiempo como un antiemético. THC o un producto combinado de THC y CBD, comercializado en algunos países como un spray oromucoso (nabiximols), puede ser una opción útil para el dolor o espasmos dolorosos en pacientes con esclerosis múltiple156, 157. El CBD puede ser eficaz en el tratamiento de algunos pacientes con epilepsia158, 159, 160, 161, pero los datos son insuficientes para proporcionar evidencia definitiva162.
Conclusiones
Como no existe un buen modelo animal de psicosis, es difícil probar de manera concluyente cualquier causa ambiental. Por lo tanto, no está claro qué cambios necesitaría inducir un cannabinoide exógeno en un animal con el fin de proporcionar una prueba definitiva de que el cannabis puede causar psicosis. Dada la falta de un equivalente de la pintura de alquitrán de tabaco en los ratones para demostrar su carcinogenicidad, ¿es razonable esperar la prueba absoluta de que los cannabinoides exógenos son una causa componente de la psicosis?
Gage et al163, que examinaron exhaustivamente la literatura epidemiológica en busca de posibles factores de confusión, sesgo, clasificación errónea, causalidad inversa y otras explicaciones para la asociación, concluyeron que "los estudios epidemiológicos proporcionan pruebas suficientes para justificar un mensaje de salud pública de que el uso de cannabis puede aumentar el riesgo de Trastornos psicóticos".
Por supuesto, es importante no exagerar nuestro conocimiento en cualquier campaña de salud pública. Por ejemplo, todavía existe incertidumbre sobre la medida en que el consumo de cannabis puede inducir psicosis en ausencia de vulnerabilidad genética. Sigue habiendo discusión sobre la proporción de la psicosis que se podría prevenir si nadie consume cannabis; las estimaciones oscilan entre el 8 y el 24% 66. Los efectos del cannabis en el cerebro también deben ser aclarados. Además, debemos velar por que la educación pública no se confunda con el debate, altamente acusado a favor y en contra de la despenalización o la legalización164.
Referencias
1. Room R. Cannabis policy: moving beyond stalemate. Oxford: Oxford University Press, 2010.
2. United Nations Office on Drugs and Crime. World drug report 2015. New York: United Nations, 2015.
3. Room R. Legalizing a market for cannabis for pleasure: Colorado, Washington, Uruguay and beyond. Addiction 2014;109:345‐51.
4. Hanus LO. Pharmacological and therapeutic secrets of plant and brain (endo)cannabinoids. Med Res Rev2009;29:213‐71. [*]
5. Mechoulam R, Parker LA. The endocannabinoid system and the brain. Annu Rev Psychol 2013;64:21‐47.[*]
6. Howlett AC, Bidaut‐Russell M, Devane WA et al. The cannabinoid receptor: biochemical, anatomical and behavioral characterization. Trends Neurosci 1990;13:420‐3. [*]
7. Katona I, Freund TF. Multiple functions of endocannabinoid signaling in the brain. Annu Rev Neurosci2012;35:529‐58. [*]
8. Piomelli D. The molecular logic of endocannabinoid signalling. Nat Rev Neurosci 2003;4:873‐84.[*]
9. Pertwee RG. The diverse CB1 and CB2 receptor pharmacology of three plant cannabinoids: delta9‐tetrahydrocannabinol, cannabidiol and delta9‐tetrahydrocannabivarin. Br J Pharmacol 2008;153:199‐215.[*]
10. Lutz B. On‐demand activation of the endocannabinoid system in the control of neuronal excitability and epileptiform seizures. Biochem Pharmacol 2004;68:1691‐8. [*]
11. Bocker KB, Gerritsen J, Hunault CC et al. Cannabis with high delta9‐THC contents affects perception and visual selective attention acutely: an event‐related potential study. Pharmacol Biochem Behav2010;96:67‐74. [*]
12. D'Souza DC, Fridberg DJ, Skosnik PD et al. Dose‐related modulation of event‐related potentials to novel and target stimuli by intravenous Delta(9)‐THC in humans. Neuropsychopharmacology 2012;37:1632‐46.[*]
13. Ilan AB, Gevins A, Coleman M et al. Neurophysiological and subjective profile of marijuana with varying concentrations of cannabinoids. Behav Pharmacol 2005;16:487‐96. [*]
14. Murray RM, Morrison PD, Henquet C et al. Cannabis, the mind and society: the hash realities. Nat Rev Neurosci 2007;8:885‐95. [*]
15. Morrison PD, Nottage J, Stone JM et al. Disruption of frontal theta coherence by Delta9‐tetrahydrocannabinol is associated with positive psychotic symptoms. Neuropsychopharmacology2011;36:827‐36. [*]
16. Morgan CJ, Page E, Schaefer C et al. Cerebrospinal fluid anandamide levels, cannabis use and psychotic‐like symptoms. Br J Psychiatry 2013;202:381‐2. [*]
17. Miller LL, Cornett TL. Marijuana: dose effects on pulse rate, subjective estimates of intoxication, free recall and recognition memory. Pharmacol Biochem Behav 1978;9:573‐7. [*]
18. Tinklenberg J, Melges F, Hollister L et al. Marijuana and immediate memory. Nature 1970;226:1171‐2.[*]
19. Morrison PD, Zois V, McKeown DA et al. The acute effects of synthetic intravenous Delta9‐tetrahydrocannabinol on psychosis, mood and cognitive functioning. Psychol Med 2009;39:1607‐16.[*]
20. Hart CL, Ilan AB, Gevins A et al. Neurophysiological and cognitive effects of smoked marijuana in frequent users. Pharmacol Biochem Behav 2010;96:333‐41. [*]
21. Nordstrom BR, Hart CL. Assessing cognitive functioning in cannabis users: cannabis use history an important consideration. Neuropsychopharmacology 2006;31:2798‐9. [*]
22. Schoeler T, Bhattacharyya S. The effect of cannabis use on memory function: an update. Subst Abuse Rehabil 2013;4:11‐27. [*]
23. Hall W. What has research over the past two decades revealed about the adverse health effects of recreational cannabis use? Addiction 2015;110:19‐35. [*]
24. D'Souza DC, Abi‐Saab WM, Madonick S et al. Delta‐9‐tetrahydrocannabinol effects in schizophrenia: implications for cognition, psychosis, and addiction. Biol Psychiatry 2005;57:594‐608. [*]
25. D'Souza DC, Ranganathan M, Braley G et al. Blunted psychotomimetic and amnestic effects of delta‐9‐tetrahydrocannabinol in frequent users of cannabis. Neuropsychopharmacology 2008;33:2505‐16. [*]
26. Freeman D, Dunn G, Murray RM et al. How cannabis causes paranoia: using the intravenous administration of 9‐tetrahydrocannabinol (THC) to identify key cognitive mechanisms leading to paranoia. Schizophr Bull 2015;41:391‐9. [*]
27. Bisogno T, Hanus L, De Petrocellis L et al. Molecular targets for cannabidiol and its synthetic analogues: effect on vanilloid VR1 receptors and on the cellular uptake and enzymatic hydrolysis of anandamide. Br J Pharmacol 2001;134:845‐52. [*]
28. Thomas A, Ross RA, Saha B et al. 6"‐Azidohex‐2"‐yne‐cannabidiol: a potential neutral, competitive cannabinoid CB1 receptor antagonist. Eur J Pharmacol 2004;487:213‐21. [*]
29. Thomas A, Baillie GL, Phillips AM et al. Cannabidiol displays unexpectedly high potency as an antagonist of CB1 and CB2 receptor agonists in vitro. Br J Pharmacol 2007;150:613‐23. [*]
30. McPartland JM, Duncan M, Di Marzo V et al. Are cannabidiol and Delta(9)‐tetrahydrocannabivarin negative modulators of the endocannabinoid system? A systematic review. Br J Pharmacol 2015;172:737‐53.[*]
31. Karniol IG, Shirakawa I, Kasinski N et al. Cannabidiol interferes with the effects of delta9‐tetrahydrocannabinol in man. Eur J Pharmacol 1974;28:172‐7. [*]
32. Zuardi AW, Shirakawa I, Finkelfarb E et al. Action of cannabidiol on the anxiety and other effects produced by delta 9‐THC in normal subjects. Psychopharmacology 1982;76:245‐50. [*]
33. Hindocha C, Freeman TP, Schafer G et al. Acute effects of delta‐9‐tetrahydrocannabinol, cannabidiol and their combination on facial emotion recognition: a randomised, double‐blind, placebo‐controlled study in cannabis users. Eur Neuropsychopharmacol 2015;25:325‐34. [*]
34. Leweke FM, Schneider U, Radwan M et al. Different effects of nabilone and cannabidiol on binocular depth inversion in man. Pharmacol Biochem Behav 2000;66:175‐81. [*]
35. Englund A, Morrison PD, Nottage J et al. Cannabidiol inhibits THC‐elicited paranoid symptoms and hippocampal‐dependent memory impairment. J Psychopharmacol 2013;27:19‐27. [*]
36. Potter DJ. A review of the cultivation and processing of cannabis (Cannabis sativa L.) for production of prescription medicines in the UK. Drug Test Anal 2014;6:31‐8. [*]
37. Hardwick S, King LA. Home Office cannabis potency study 2008. St. Albans: Home Office Scientific Development Branch, 2008.
38. Pijlman FT, Rigter SM, Hoek J et al. Strong increase in total delta‐THC in cannabis preparations sold in Dutch coffee shops. Addict Biol 2005;10:171‐80. [*]
39. Swift W, Wong A, Li KM et al. Analysis of cannabis seizures in NSW, Australia: cannabis potency and cannabinoid profile. PLoS One 2013;8:e70052. [*]
40. ElSohly MA, Mehmedic Z, Foster S et al. Changes in cannabis potency over the last 2 decades (1995‐2014): analysis of current data in the United States. Biol Psychiatry 2016;79:613‐9. [*]
41. Seely KA, Lapoint J, Moran JH et al. Spice drugs are more than harmless herbal blends: a review of the pharmacology and toxicology of synthetic cannabinoids. Prog Neuropsychopharmacol Biol Psychiatry2012;39:234‐43. [*]
42. Spaderna M, Addy PH, D'Souza DC. Spicing things up: synthetic cannabinoids. Psychopharmacology2013;228:525‐40. [*]
43. European Monitoring Center for Drugs and Drug Addiction . European drug report 2016. Lisbon: European Monitoring Center for Drugs and Drug Addiction, 2016.
44. Tait RJ, Caldicott D, Mountain D et al. A systematic review of adverse events arising from the use of synthetic cannabinoids and their associated treatment. Clin Toxicol 2016;54:1‐13. [*]
45. Winstock A, Lynskey M, Borschmann R, et al. Risk of emergency medical treatment following consumption of cannabis or synthetic cannabinoids in a large global sample. J Psychopharmacol2015;29:698‐703. [*]
46. Schifano F, Orsolini L, Duccio Papanti G et al. Novel psychoactive substances of interest for psychiatry. World Psychiatry 2015;14:15‐26. [*]
47. Clouston TS. The Cairo Asylum − Dr. Warnock on hasheesh insanity. Br J Psychiatry 1896;42:790‐5.
48. Andréasson S, Engström A, Allebeck P et al. Cannabis and schizophrenia. A longitudinal study of Swedish conscripts. Lancet 1987;330:1483‐6. [*]
49. Anonymous . Deglamorising cannabis. Lancet 1995;346:1241. [*]
50. Gage SH, Hickman M, Zammit S. Association between cannabis and psychosis: epidemiologic evidence. Biol Psychiatry 2016;79:549‐56. [*]
51. Murray RM, Di Forti M. Cannabis and psychosis: what degree of proof do we require? Biol Psychiatry2016;79:514‐5. [*]
52. Tien AY, Anthony JC. Epidemiological analysis of alcohol and drug use as risk factors for psychotic experiences. J Nerv Ment Dis 1990;178:473‐80. [*]
53. Zammit S, Allebeck P, Andréasson S et al. Self reported cannabis use as a risk factor for schizophrenia in Swedish conscripts of 1969: historical cohort study. BMJ 2002;325:1199. [*]
54. Manrique‐Garcia E, Zammit S, Dalman C et al. Cannabis, schizophrenia and other non‐affective psychoses: 35 years of follow‐up of a population‐based cohort. Psychol Med 2012;42:1321‐8. [*]
55. van Os J, Bak M, Hanssen M et al. Cannabis use and psychosis: a longitudinal population‐based study. Am J Epidemiol 2002;156:319‐27. [*]
56. Weiser M, Knobler HY, Noy S et al. Clinical characteristics of adolescents later hospitalized for schizophrenia. Am J Med Genet 2002;114:949‐55. [*]
57. Fergusson DM, Horwood LJ, Swain‐Campbell NR. Cannabis dependence and psychotic symptoms in young people. Psychol Med 2003;33:15‐21. [*]
58. Arseneault L, Cannon M, Poulton R et al. Cannabis use in adolescence and risk for adult psychosis: longitudinal prospective study. BMJ 2002;325:1212‐3. [*]
59. Ferdinand RF, Sondeijker F, van der Ende J et al. Cannabis use predicts future psychotic symptoms, and vice versa. Addiction 2005;100:612‐8. [*]
60. Henquet C, Krabbendam L, Spauwen J et al. Prospective cohort study of cannabis use, predisposition for psychosis, and psychotic symptoms in young people. BMJ 2005;330:11. [*]
61. Wiles NJ, Zammit S, Bebbington P et al. Self‐reported psychotic symptoms in the general population: results from the longitudinal study of the British National Psychiatric Morbidity Survey. Br J Psychiatry2006;188:519‐26. [*]
62. Rössler W, Hengartner MP, Angst J et al. Linking substance use with symptoms of subclinical psychosis in a community cohort over 30 years. Addiction 2012;107:1174‐84. [*]
63. Gage SH, Hickman M, Heron J et al. Associations of cannabis and cigarette use with psychotic experiences at age 18: findings from the Avon Longitudinal Study of Parents and Children. Psychol Med2014;44:3435‐44. [*]
64. Rognli EB, Berge J, Håkansson A et al. Long‐term risk factors for substance‐induced and primary psychosis after release from prison. A longitudinal study of substance users. Schizophr Res 2015;168:185‐90. [*]
65. Marconi A, Di Forti M, Lewis CM et al. Meta‐analysis of the association between the level of cannabis use and risk of psychosis. Schizophr Bull 2016;42:1262‐9. [*]
66. Di Forti M, Marconi A, Carra E et al. Proportion of patients in south London with first‐episode psychosis attributable to use of high potency cannabis: a case‐control study. Lancet Psychiatry 2015;2:233‐8. [*]
67. Di Forti M, Morgan C, Dazzan P et al. High‐potency cannabis and the risk of psychosis. Br J Psychiatry2009;195:488‐91. [*]
68. Di Forti M, Sallis H, Allegri F et al. Daily use, especially of high‐potency cannabis, drives the earlier onset of psychosis in cannabis users. Schizophr Bull 2014;40:1509‐17. [*]
69. Schubart CD, Sommer IE, van Gastel WA et al. Cannabis with high cannabidiol content is associated with fewer psychotic experiences. Schizophr Res 2011;130:216‐21. [*]
70. Morgan CJ, Curran HV. Effects of cannabidiol on schizophrenia‐like symptoms in people who use cannabis. Br J Psychiatry 2008;192:306‐7. [*]
71. Pierre JM, Gandal M, Son M. Cannabis‐induced psychosis associated with high potency "wax dabs". Schizophr Res 2016;172:211‐2. [*]
72. Castaneto MS, Gorelick DA, Desrosiers NA et al. Synthetic cannabinoids: epidemiology, pharmacodynamics, and clinical implications. Drug Alcohol Depend 2014;144:12‐41. [*]
73. Papanti D, Schifano F, Botteon G et al. "Spiceophrenia": a systematic overview of "spice"‐related psychopathological issues and a case report. Hum Psychopharmacol 2013;28:379‐89. [*]
74. Fattore L. Synthetic cannabinoids − further evidence supporting the relationship between cannabinoids and psychosis. Biol Psychiatry 2016;79:539‐48. [*]
75. Large M, Sharma S, Compton MT et al. Cannabis use and earlier onset of psychosis: a systematic meta‐analysis. Arch Gen Psychiatry 2011;68:555‐61. [*]
76. Loberg EM, Helle S, Nygard M et al. The cannabis pathway to non‐affective psychosis may reflect less neurobiological vulnerability. Front Psychiatry 2014;5:159. [*]
77. Arnold C, Allott K, Farhall J et al. Neurocognitive and social cognitive predictors of cannabis use in first‐episode psychosis. Schizophr Res 2015;168:231‐7. [*]
78. Ferraro L, Russo M, O'Connor J et al. Cannabis users have higher premorbid IQ than other patients with first onset psychosis. Schizophr Res 2013;150:129‐35. [*]
79. Ruiz‐Veguilla M, Callado LF, Ferrin M. Neurological soft signs in patients with psychosis and cannabis abuse: a systematic review and meta‐analysis of paradox. Curr Pharm Des 2012;18:5156‐64. [*]
80. Ksir C, Hart CL. Cannabis and psychosis: a critical overview of the relationship. Curr Psychiatry Rep2016;18:12. [*]
81. Hill M. Perspective: Be clear about the real risks. Nature 2015;525:S14. [*]
82. Haney M, Evins AE. Does cannabis cause, exacerbate or ameliorate psychiatric disorders? An oversimplified debate discussed. Neuropsychopharmacology 2016;41:393‐401. [*]
83. Fergusson DM, Boden JM, Horwood LJ. Psychosocial sequelae of cannabis use and implications for policy: findings from the Christchurch Health and Development Study. Soc Psychiatry Psychiatr Epidemiol2015;50:1317‐26. [*]
84. Bianconi F, Bonomo M, Marconi A et al. Differences in cannabis‐related experiences between patients with a first episode of psychosis and controls. Psychol Med 2016;46:995‐1003. [*]
85. Boydell J, van Os J, Caspi A et al. Trends in cannabis use prior to first presentation with schizophrenia, in South‐East London between 1965 and 1999. Psychol Med 2006;36:1441‐6. [*]
86. Ksir C, Hart CL. Correlation still does not imply causation. Lancet Psychiatry 2016;3:401. [*]
87. McGuire PK, Jones P, Harvey I et al. Morbid risk of schizophrenia for relatives of patients with cannabis‐associated psychosis. Schizophr Res 1995;15:277‐81. [*]
88. Power RA, Verweij KJ, Zuhair M et al. Genetic predisposition to schizophrenia associated with increased use of cannabis. Mol Psychiatry 2014;19:1201‐4. [*]
89. Gage SH, Munafò MR, MacLeod J et al. Cannabis and psychosis. Lancet Psychiatry 2015;2:380.[*]
90. Di Forti M, Vassos E, Lynskey M et al. Cannabis and psychosis ‐ Authors' reply. Lancet Psychiatry2015;2:382. [*]
91. Martin AK, Robinson G, Reutens D et al. Cannabis abuse and age at onset in schizophrenia patients with large, rare copy number variants. Schizophr Res 2014;155:21‐5. [*]
92. Caspi A, Moffitt TE, Cannon M et al. Moderation of the effect of adolescent‐onset cannabis use on adult psychosis by a functional polymorphism in the catechol‐O‐methyltransferase gene: longitudinal evidence of a gene x environment interaction. Biol Psychiatry 2005;57:1117‐27. [*]
93. Tunbridge EM, Dunn G, Murray RM et al. Genetic moderation of the effects of cannabis: catechol‐O‐methyltransferase (COMT) affects the impact of Delta9‐tetrahydrocannabinol (THC) on working memory performance but not on the occurrence of psychotic experiences. J Psychopharmacol 2015;29:1146‐51.[*]
94. van Winkel R, van Beveren NJ, Simons C. AKT1 moderation of cannabis‐induced cognitive alterations in psychotic disorder. Neuropsychopharmacology 2011;36:2529‐37. [*]
95. Di Forti M, Iyegbe C, Sallis H et al. Confirmation that the AKT1 (rs2494732) genotype influences the risk of psychosis in cannabis users. Biol Psychiatry 2012;72:811‐6. [*]
96. Morgan CJ, Freeman TP, Powell J et al. AKT1 genotype moderates the acute psychotomimetic effects of naturalistically smoked cannabis in young cannabis smokers. Transl Psychiatry 2016;6:e738. [*]
97. Colizzi M, Iyegbe C, Powell J et al. Interaction between functional genetic variation of DRD2 and cannabis use on risk of psychosis. Schizophr Bull 2015;41:1171‐82. [*]
98. Gill KE, Poe L, Azimov N et al. Reasons for cannabis use among youths at ultra high risk for psychosis. Early Interv Psychiatry 2015;9:207‐10. [*]
99. Bossong MG, Mehta MA, van Berckel BN et al. Further human evidence for striatal dopamine release induced by administration of 9‐tetrahydrocannabinol (THC): selectivity to limbic striatum. Psychopharmacology 2015;232:2723‐9. [*]
100. Volkow ND, Wang GJ, Telang F et al. Decreased dopamine brain reactivity in marijuana abusers is associated with negative emotionality and addiction severity. Proc Natl Acad Sci USA 2014;111:E3149‐56.[*]
101. Murray RM, Mehta M, Di Forti M. Different dopaminergic abnormalities underlie cannabis dependence and cannabis‐induced psychosis. Biol Psychiatry 2014;75:430‐1. [*]
102. Ginovart N, Tournier BB, Moulin‐Sallanon M, et al. Chronic Delta(9)‐tetrahydrocannabinol exposure induces a sensitization of dopamine D(2)/(3) receptors in the mesoaccumbens and nigrostriatal systems. Neuropsychopharmacology 2012;37:2355‐67. [*]
103. Schoeler T, Monk A, Sami MB et al. Continued versus discontinued cannabis use in patients with psychosis: a systematic review and meta‐analysis. Lancet Psychiatry 2016;3:215‐25. [*]
104. Brunette MF, Dawson R, O'Keefe CD et al. A randomized trial of clozapine vs. other antipsychotics for cannabis use disorder in patients with schizophrenia. J Dual Diagn 2011;7:50‐63. [*]
105. Budney AJ, Roffman R, Stephens RS et al. Marijuana dependence and its treatment. Addict Sci Clin Pract 2007;4:4‐16. [*]
106. Lopez‐Quintero C, Perez de los Cobos J, Hasin DS et al. Probability and predictors of transition from first use to dependence on nicotine, alcohol, cannabis, and cocaine: results of the National Epidemiologic Survey on Alcohol and Related Conditions (NESARC). Drug Alcohol Depend 2011;115:120‐30. [*]
107. Anthony J. The epidemiology of cannabis dependence In: Roffman RA, editor; , Stephens RS, editor. (eds). Cannabis dependence: its nature, consequences and treatment. Cambridge: Cambridge University Press, 2006:58‐105.
108. Health & Social Care Information Centre. Statistics on drug misuse. England 2014. London: Health & Social Care Information Centre, 2014.
109. Freeman T, Winstock A. Examining the profile of high‐potency cannabis and its association with severity of cannabis dependence. Psychol Med 2015;45:3181‐9. [*]
110. Toftdahl NG, Nordentoft M, Hjorthøj C. Prevalence of substance use disorders in psychiatric patients: a nationwide Danish population‐based study. Soc Psychiatry Psychiatr Epidemiol 2016;51:129‐40. [*]
111. Degenhardt L, Hall W, Lynskey M. The relationship between cannabis use, depression and anxiety among Australian adults: findings from the National Survey of Mental Health and Well‐Being. Soc Psychiatry Psychiatr Epidemiol 2001;36:219‐27. [*]
112. Feingold D, Weiser M, Rehm J et al. The association between cannabis use and anxiety disorders: results from a population‐based representative sample. Eur Neuropsychopharmacol 2016;26:493‐505.[*]
113. Kedzior KK, Laeber LT. A positive association between anxiety disorders and cannabis use or cannabis use disorders in the general population − a meta‐analysis of 31 studies. BMC Psychiatry 2014;14:1‐22.[PMC free article] [*]
114. Chen C‐Y, Wagner AF, Anthony CJ. Marijuana use and the risk of major depressive episode. Soc Psychiatry Psychiatr Epidemiol 2002;37:199‐206. [*]
115. Feingold D, Weiser M, Rehm J et al. The association between cannabis use and mood disorders: a longitudinal study. J Affect Disord 2015;172:211‐8. [*]
116. Crippa JA, Zuardi AW, Martín‐Santos R et al. Cannabis and anxiety: a critical review of the evidence. Hum Psychopharmacol 2009;24:515‐23
117. Manrique‐Garcia E, Zammit S, Dalman C et al. Cannabis use and depression: a longitudinal study of a national cohort of Swedish conscripts. BMC Psychiatry 2012;12:112.
118. Degenhardt L, Hall W, Lynskey M. Exploring the association between cannabis use and depression. Addiction 2003;98:1493‐504.
119. Moore THM, Zammit S, Lingford‐Hughes A et al. Cannabis use and risk of psychotic or affective mental health outcomes: a systematic review. Lancet 2007;370:319‐28.
120. Lev‐Ran S, Roerecke M, Le Foll B et al. The association between cannabis use and depression: a systematic review and meta‐analysis of longitudinal studies. Psychol Med 2014;44:797‐810.
121. Blanco C, Hasin DS, Wall MM et al. Cannabis use and risk of psychiatric disorders: prospective evidence from a US national longitudinal study. JAMA Psychiatry 2016;73:388‐95.
122. Cougle JR, Bonn‐Miller MO, Vujanovic AA et al. Posttraumatic stress disorder and cannabis use in a nationally representative sample. Psychol Addict Behav 2011;25:554‐8.
123. Kevorkian S, Bonn‐Miller MO, Belendiuk K et al. Associations among trauma, posttraumatic stress disorder, cannabis use, and cannabis use disorder in a nationally representative epidemiologic sample. Psychol Addict Behav 2015;29:633‐8.
124. Kilpatrick DG, Acierno R, Saunders B et al. Risk factors for adolescent substance abuse and dependence: data from a national sample. J Consult Clin Psychol 2000;68:19‐30.
125. Chilcoat HD, Breslau N. Posttraumatic stress disorder and drug disorders: testing causal pathways. Arch Gen Psychiatry 1998;55:913‐7.
126. Vlahov D, Galea S, Resnick H et al. Increased use of cigarettes, alcohol, and marijuana among Manhattan, New York, residents after the September 11th terrorist attacks. Am J Epidemiol 2002;155:988‐96.
127. Notzon DP, Pavlicova M, Glass A et al. ADHD is highly prevalent in patients seeking treatment for cannabis use disorders. J Atten Disord (in press).
128. Fergusson DM, Boden JM. Cannabis use and adult ADHD symptoms. Drug Alcohol Depend2008;95:90‐6.
129. Chang Z, Lichtenstein P, Larsson H. The effects of childhood ADHD symptoms on early‐onset substance use: a Swedish twin study. J Abnorm Child Psychol 2012;40:425‐35
130. Experimental Medicine in ADHD − Cannabinoids (EMA‐C). https://clinicaltrials.gov/.
131. Weiland BJ, Thayer RE, Depue BE et al. Daily marijuana use is not associated with brain morphometric measures in adolescents or adults. J Neurosci 2015;35:1505‐12.
132. French L, Gray C, Leonard G et al. Early cannabis use, polygenic risk score for schizophrenia and brain maturation in adolescence. JAMA Psychiatry 2015;72:1002‐11.
133. Pagliaccio D, Barch DM, Bogdan R et al. Shared predisposition in the association between cannabis use and subcortical brain structure. JAMA Psychiatry 2015;72:994‐1001.
134. Yucel M, Lorenzetti V, Suo C et al. Hippocampal harms, protection and recovery following regular cannabis use. Transl Psychiatry 2016;6:e710.
135. Demirakca T, Sartorius A, Ende G et al. Diminished gray matter in the hippocampus of cannabis users: possible protective effects of cannabidiol. Drug Alcohol Depend 2011;114:242‐5.
136. Rigucci S, Marques TR, Di Forti M et al. Effect of high‐potency cannabis on corpus callosum microstructure. Psychol Med 2016;46:841‐54.
137. Schoeler T, Kambeitz J, Behlke I et al. The effects of cannabis on memory function in users with and without a psychotic disorder: findings from a combined meta‐analysis. Psychol Med 2016;46:177‐88.
138. Volkow ND, Swanson JM, Evins AE et al. Effects of cannabis use on human behavior, including cognition, motivation, and psychosis: a review. JAMA Psychiatry 2016;73:292‐7.
139. Meier MH, Caspi A, Ambler A, et al. Persistent cannabis users show neuropsychological decline from childhood to midlife. Proc Natl Acad Sci USA 2012;109:E2657‐64.
140. Mokrysz C, Landy R, Gage SH et al. Are IQ and educational outcomes in teenagers related to their cannabis use? A prospective cohort study. J Psychopharmacol 2016;30:159‐68.
141. Jackson NJ, Isen JD, Khoddam R et al. Impact of adolescent marijuana use on intelligence: results from two longitudinal twin studies. Proc Natl Acad Sci USA 2016;113:E500‐8.
142. Auer R, Vittinghoff E, Yaffe K et al. association between lifetime marijuana use and cognitive function in middle age: the Coronary Artery Risk Development in Young Adults (CARDIA) Study. JAMA Intern Med 2016;176:352‐61.
143. Hall W, Lynskey M. Long‐term marijuana use and cognitive impairment in middle age. JAMA Intern Med 2016;176:362‐3.
144. Schreiner AM, Dunn ME. Residual effects of cannabis use on neurocognitive performance after prolonged abstinence: a meta‐analysis. Exp Clin Psychopharmacol 2012;20:420‐9.
145. Morgan CJ, Schafer G, Freeman TP et al. Impact of cannabidiol on the acute memory and psychotomimetic effects of smoked cannabis: naturalistic study. Br J Psychiatry 2010;197:285‐90.
146. Morgan CJ, Gardener C, Schafer G et al. Sub‐chronic impact of cannabinoids in street cannabis on cognition, psychotic‐like symptoms and psychological well‐being. Psychol Med 2012;42:391‐400.
147. Pope HG Jr, Gruber AJ, Hudson JI et al. Early‐onset cannabis use and cognitive deficits: what is the nature of the association? Drug Alcohol Depend 2003;69:303‐10.
148. Meier MH, Hill ML, Small PJ et al. Associations of adolescent cannabis use with academic performance and mental health: a longitudinal study of upper middle class youth. Drug Alcohol Depend2015;156:207‐12.
149. Cerdá M, Moffitt TE, Meier MH et al. Persistent cannabis dependence and alcohol dependence represent risks for midlife economic and social problems: a longitudinal cohort study. Clin Psychol Sci (in press).
150. Silins E, Horwood LJ, Patton GC et al. Young adult sequelae of adolescent cannabis use: an integrative analysis. Lancet Psychiatry 2014;1:286‐93.
151. Stiby AI, Hickman M, Munafo MR et al. Adolescent cannabis and tobacco use and educational outcomes at age 16: birth cohort study. Addiction 2015;110:658‐68.
152. Leweke FM, Piomelli D, Pahlisch F et al. Cannabidiol enhances anandamide signaling and alleviates psychotic symptoms of schizophrenia. Transl Psychiatry 2012;2:e94.
153. McGuire P. A double‐blind, randomised, placebo‐controlled, parallel group trial of cannabidiol as adjunctive therapy in the first line treatment of schizophrenia or related psychotic disorder. Presented at the 5th Schizophrenia International Research Society Conference, Florence, April 2016.
154. Abrams DI, Jay C, Shade S et al. Cannabis in painful HIV‐associated sensory neuropathy. A randomized placebo‐controlled trial. Neurology 2007;68:515‐21.
155. Andreae MH, Carter GM, Shaparin N et al. Inhaled cannabis for chronic neuropathic pain: a meta‐analysis of individual patient data. J Pain 2015;16:1221‐32.
156. Patti F, Messina S, Solaro C et al. Efficacy and safety of cannabinoid oromucosal spray for multiple sclerosis spasticity. J Neurol Neurosurg Psychiatry 2016;87:944‐51.
157. Koppel BS, Brust JCM, Fife T et al. Systematic review: Efficacy and safety of medical marijuana in selected neurologic disorders: Report of the Guideline Development Subcommittee of the American Academy of Neurology. Neurology 2014;82:1556‐63.
158. Brust JC, Ng SK, Hauser AW et al. Marijuana use and the risk of new onset seizures. Transactions of the American Clinical and Climatological Association 1992;103:176‐81.
159. Gloss D, Vickrey B. Cannabinoids for epilepsy. Cochrane Database Syst Rev 2012;6.
160. Porter BE, Jacobson C. Report of a parent survey of cannabidiol‐enriched cannabis use in pediatric treatment‐resistant epilepsy. Epilepsy Behav 2013;29:574‐7.
161. Press CA, Knupp KG, Chapman KE. Parental reporting of response to oral cannabis extracts for treatment of refractory epilepsy. Epilepsy Behav 2015;45:49‐52.
162. Friedman D, Devinsky O. Cannabinoids in the treatment of epilepsy. N Engl J Med 2015;373:1048‐58.
163. Gage SH, Hickman M, Zammit S. Association between cannabis and psychosis: epidemiologic evidence. Biol Psychiatry 2016;79:549‐56
164. Large M. The need for health warnings about cannabis and psychosis. Lancet Psychiatry 2016;3:188‐9.
165. Hasin DS, Wall M, Keyes KM et al. Medical marijuana laws and adolescent marijuana use in the USA from 1991 to 2014: results from annual, repeated cross‐sectional surveys. Lancet Psychiatry 2015;2:601‐8
166. Shi Y, Lenzi M, An R. Cannabis liberalization and adolescent cannabis use: a cross‐national study in 38 countries. PLoS One 2015;10:e0143562.
Traducción del articulo publicado en la revista digital NCBI (US National Library of Medicine National Institutes of Health) el 22 de septiembre del 2016 en su version en linea. La autoría del artículo corresponde a Robin M. Murray, Harriet Quigley, Diego Quattrone, Amir Englund y Marta Di Forti. Todos los derechos reservados.
Traducción realizada por Totól Achipahuatl para el Colectivo Salud Crónica el 19 de junio del 2017.
